ჰარვარდის სამედიცინო სკოლის (HMS) და MIT-ის ზოგადი საავადმყოფოს ერთობლივი კვლევითი ჯგუფის განცხადებით, მათ PEC გრავირების მეთოდის გამოყენებით მიკროდისკის ლაზერის გამომავალი სიმძლავრის რეგულირება შეძლეს, რაც ნანოფოტონიკისა და ბიომედიცინის ახალ წყაროს „პერსპექტიულს“ ხდის.
(მიკროდისკის ლაზერის გამომავალი სიგნალის რეგულირება შესაძლებელია PEC გრავირების მეთოდით)
სფეროებშინანოფოტონიკადა ბიომედიცინა, მიკროდისკილაზერებიდა ნანოდისკის ლაზერები პერსპექტიული გახდასინათლის წყაროებიდა ზონდები. რამდენიმე გამოყენებაში, როგორიცაა ჩიპზე დაფუძნებული ფოტონური კომუნიკაცია, ჩიპზე დაფუძნებული ბიოვიზუალიზაცია, ბიოქიმიური ზონდირება და კვანტური ფოტონის ინფორმაციის დამუშავება, მათ სჭირდებათ ლაზერული გამომავალი სიხშირის მიღწევა ტალღის სიგრძისა და ულტრავიწრო ზოლის სიზუსტის დასადგენად. თუმცა, ამ ზუსტი ტალღის სიგრძის მიკროდისკებისა და ნანოდისკების ლაზერების წარმოება დიდი მასშტაბით კვლავ რთულია. ნანოწარმოების მიმდინარე პროცესები შემოაქვს დისკის დიამეტრის შემთხვევითობას, რაც ართულებს ლაზერული მასის დამუშავებასა და წარმოებაში ფიქსირებული ტალღის სიგრძის მიღებას. ახლა, ჰარვარდის სამედიცინო სკოლისა და მასაჩუსეტსის ზოგადი საავადმყოფოს ველმანის ცენტრის მკვლევართა გუნდი...ოპტოელექტრონული მედიცინაშეიმუშავა ინოვაციური ოპტოქიმიური (PEC) გრავირების ტექნიკა, რომელიც ხელს უწყობს მიკროდისკის ლაზერის ლაზერული ტალღის სიგრძის ზუსტად რეგულირებას სუბნანომეტრის სიზუსტით. ნაშრომი გამოქვეყნებულია ჟურნალ „Advanced Photonics“-ში.
ფოტოქიმიური გრავირება
ცნობების თანახმად, გუნდის ახალი მეთოდი საშუალებას იძლევა წარმოიქმნას მიკროდისკების ლაზერები და ნანოდისკების ლაზერული მასივები ზუსტი, წინასწარ განსაზღვრული ემისიის ტალღის სიგრძით. ამ გარღვევის გასაღები PEC გრავირების გამოყენებაა, რომელიც უზრუნველყოფს მიკროდისკების ლაზერის ტალღის სიგრძის დახვეწის ეფექტურ და მასშტაბირებად გზას. ზემოთ მოცემულ შედეგებში, გუნდმა წარმატებით მიიღო ინდიუმის გალიუმის არსენიდის ფოსფატირების მიკროდისკები, რომლებიც დაფარული იყო სილიციუმით ინდიუმის ფოსფიდის სვეტის სტრუქტურაზე. შემდეგ მათ ამ მიკროდისკების ლაზერული ტალღის სიგრძე ზუსტად დაარეგულირეს განსაზღვრულ მნიშვნელობამდე გოგირდმჟავას განზავებულ ხსნარში ფოტოქიმიური გრავირების შესრულებით.
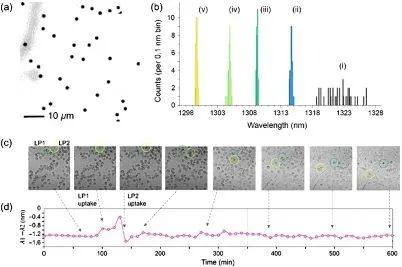
მათ ასევე შეისწავლეს სპეციფიკური ფოტოქიმიური (PEC) გრავირების მექანიზმები და დინამიკა. და ბოლოს, მათ ტალღის სიგრძეზე მორგებული მიკროდისკების მასივი გადაიტანეს პოლიდიმეთილსილოქსანის სუბსტრატზე, რათა მიეღოთ დამოუკიდებელი, იზოლირებული ლაზერული ნაწილაკები სხვადასხვა ლაზერული ტალღის სიგრძით. შედეგად მიღებული მიკროდისკი აჩვენებს ლაზერული გამოსხივების ულტრაფართოზოლოვან გამტარობას,ლაზერისვეტზე 0.6 ნმ-ზე ნაკლები და იზოლირებული ნაწილაკი 1.5 ნმ-ზე ნაკლები.
ბიოსამედიცინო აპლიკაციების კარის გაღება
ეს შედეგი კარს უხსნის ნანოფოტონიკისა და ბიოსამედიცინო გამოყენების მრავალ ახალ სფეროს. მაგალითად, დამოუკიდებელი მიკროდისკის ლაზერები შეიძლება გამოყენებულ იქნას როგორც ფიზიკურ-ოპტიკური შტრიხკოდები ჰეტეროგენული ბიოლოგიური ნიმუშებისთვის, რაც შესაძლებელს ხდის კონკრეტული უჯრედების ტიპების მარკირებას და სპეციფიკური მოლეკულების დამიზნებას მულტიპლექსურ ანალიზში. უჯრედის ტიპ-სპეციფიკური მარკირება ამჟამად ხორციელდება ჩვეულებრივი ბიომარკერების გამოყენებით, როგორიცაა ორგანული ფლუოროფორები, კვანტური წერტილები და ფლუორესცენტური მძივები, რომლებსაც აქვთ ფართო ემისიის ხაზის სიგანე. ამრიგად, ერთდროულად მხოლოდ რამდენიმე სპეციფიკური უჯრედის ტიპის მარკირებაა შესაძლებელი. ამის საპირისპიროდ, მიკროდისკის ლაზერის ულტრავიწროზოლიანი სინათლის გამოსხივება ერთდროულად მეტი უჯრედის ტიპის იდენტიფიცირებას შეძლებს.
გუნდმა გამოსცადა და წარმატებით აჩვენა ზუსტად მორგებული მიკროდისკის ლაზერული ნაწილაკები, როგორც ბიომარკერები, მათი გამოყენებით კულტივირებული ნორმალური სარძევე ჯირკვლის ეპითელური უჯრედების MCF10A მარკირებისთვის. მათი ულტრაფართოზოლოვანი გამოსხივებით, ამ ლაზერებს შეუძლიათ პოტენციურად რევოლუცია მოახდინონ ბიოსენსორულ სფეროში, ისეთი დადასტურებული ბიოსამედიცინო და ოპტიკური ტექნიკის გამოყენებით, როგორიცაა ციტოდინამიკური ვიზუალიზაცია, ნაკადური ციტომეტრია და მულტი-ომიკური ანალიზი. PEC გრავირებაზე დაფუძნებული ტექნოლოგია მიკროდისკის ლაზერების სფეროში მნიშვნელოვან წინსვლას წარმოადგენს. მეთოდის მასშტაბირება, ისევე როგორც მისი სუბნანომეტრიული სიზუსტე, ახალ შესაძლებლობებს ქმნის ლაზერების უამრავი გამოყენებისთვის ნანოფოტონიკასა და ბიოსამედიცინო მოწყობილობებში, ასევე შტრიხკოდების შესაქმნელად კონკრეტული უჯრედული პოპულაციებისა და ანალიტიკური მოლეკულებისთვის.
გამოქვეყნების დრო: 2024 წლის 29 იანვარი





